基因體,乃人類生命的藍圖,包含三十億組鹼基對、兩萬五千個基因,十萬分的複雜。其結構上的缺失或基因表現的異常,釀成許多人類疾病。理解各別基因的功能與他們之間互動的模式,是解開生命謎團的關鍵,使人類得以發展疾病治療策略。長久以來,科學家夢想有朝一日可以精準有效率地修正特定基因,並且「編輯」剔除有缺陷的基因。感謝今年唐獎生技醫藥獎得主們,「有朝一日」便是「今日」。
基因體的複雜程度,使得在核苷酸層次進行特定基因的編輯,好比大海撈針。過去曾發展數種方式可以進行基因體編輯,但是由今年得獎者,伊曼紐‧夏彭提耶博士、珍妮佛‧道納博士和張鋒博士等人所開發的CRISPR/Cas9平台,在效率、精準度和敏銳度上,大勝以往。CRISPR/Cas(常間回文重複序列叢集/常間回文重複序列叢集關聯蛋白系統)是細菌和古菌對抗外來入侵DNA的適應性免疫防禦系統(例如噬菌體感染時)。Cas9蛋白是一種可以剪斷DNA的核酸內切酶。過去幾年,科學家對Cas9大感興趣,爭相將此原核生物的核酸酶,轉變成真核生物也適用的靈活基因體編輯工具。
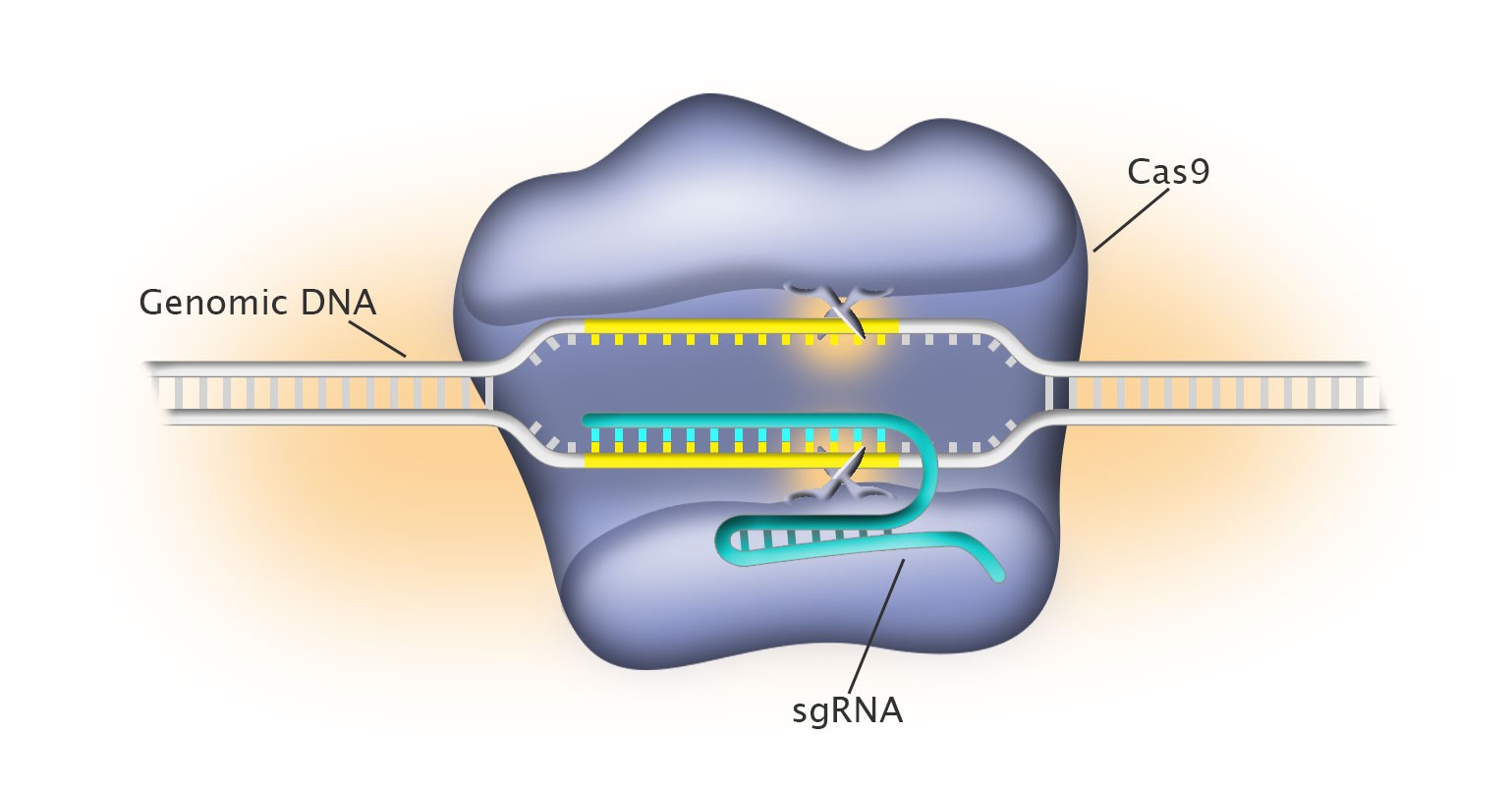
Cas9好比一副剪刀,可以精準剪斷一串珍珠。這串珍珠是我們的DNA(或基因體),有三十億顆珍珠(核苷酸)。要從三十億顆珍珠當中,挑出特定的某一顆來剪,難如登天。然而Cas9配有一套「GPS導航系統」,可以由某些類型的RNA將Cas9導向目標DNA。夏彭提耶博士率先發現有兩種RNA負責此工作:CRISPR RNA(crRNA)及反式激活crRNA(tracrRNA)。和夏彭提耶博士合作的道納博士則發現這兩個RNA可以嵌合在一起,形成可以客製化的單鏈引導RNA(sgRNA)去找尋目標基因。夏彭提耶博士和道納博士所發展的雙分子系統(Cas9和sgRNA)大幅度減化實驗步驟,使基因體編輯更有效率。同一時間,張鋒博士對Cas9系統進行自己獨立的改良實驗,率先在哺乳類和人類細胞進行成功的基因體編輯。而後更進一步改良「同時編輯多個基因」、以及「同源性基因修復」的實驗方法。這三位傑出科學家的成就,大幅改革了基因體編輯平台,使其程式化、普及化、並且得以量化。自從2012和2013年刊出以來,全球上百乃至上千間實驗室皆利用此平台進行人類及各種生物細胞的遺傳工程,包括:斑馬魚、植物、猴子、豬和小鼠。許多人相信這是繼基因選殖技術(cloning)和聚合酶連鎖反應(PCR)以來,基因體研究史上最偉大的科技發展之一。
除了切割和修復基因之外,經過修飾的Cas9甚至可用來活化或抑制特定的基因。Cas9系統已改變人們做遺傳實驗的方法,更是將研發的閘門大開,造福人類的疾病新療法,將如滔滔江水,連綿不絕。一些可能的應用包括:各種遺傳疾病的治療,用以修復缺失基因,例如鐮狀細胞性貧血;修復導致癌症的突變基因;清除慢性病毒感染細胞所造成的嵌合基因,例如人類免疫缺陷病毒(HIV)感染。此技術甚至可以用在人類幹細胞工程,以研究疾病模式、篩選藥物、辨識細胞分化過程中必要的基因、抑癌基因、調控細胞分化的基因、或容易被病毒或其他病原感染的基因等。其潛力無窮,唯有被想像力所侷限。駕馭此革命性技術以提升人類健康的計畫已在進行,巨幅的影響力指日可待。
伊曼紐‧夏彭提耶博士,一位法籍微生物學家,在病原細菌的感染與免疫調控機制研究上,被公認為世界首屈一指的專家。現職為德國馬克斯‧普朗克傳染病生物學研究所(Max Planck Institute for Infection Biology),傳染病生物學調控部門的部長。在CRISPR的發展中,其主要的貢獻在於發現Cas9蛋白的活性仰賴tracrRNA。
珍妮佛‧道納博士在美國加州大學柏克萊分校(University of California, Berkeley),擔任化學及分子暨細胞生物學系教授,是霍華德‧休斯醫學研究所(HHMI)的研究員,同時也是美國國家科學院院士。身為著名的RNA結構生物學家,他曾研究核酶、內轉譯子(IRES)、和較後來的Cas9/RNA交互作用。crRNA與tracrRNA可以融合成單鏈引導RNA(sgRNA)辨識目標序列,被認為是他和夏彭提耶博士的共同功勞。
張鋒博士任職麻省理工學院(MIT),是麥戈文腦科學研究所(McGovern Institute for Brain Research)的研究員、博德研究所(Broad Institute)的核心成員,且在MIT擔任腦與認知科學及生物工程副教授。他出生於中國,十一歲搬去美國,是一位華裔美籍生物工程學家,致力於開發工具來研究神經科學與人類疾病。他先前的研究造就了「光遺傳學」科技,應用在神經細胞的再生。在CRISPR技術的發展中,其主要的貢獻在於率先使其適用於哺乳類細胞。



